本文來自微信公眾號:英為財情Investing,作者:莫寧。
輝瑞和BioNTech公布了積極的新冠疫苗初步試驗結果,提醒市場疫苗競賽已經進入到關鍵衝刺階段。未來幾周,市場預計會接收到有關疫苗的更多進展。
目前,有五款疫苗處於領先位置,其中輝瑞和Moderna被認為會是第一批獲得FDA緊急使用授權的公司。以下為這五款疫苗當前的研發狀態。
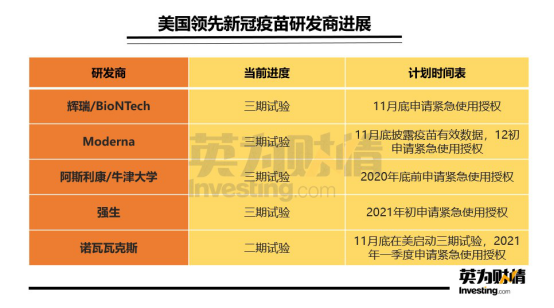
輝瑞疫苗BNT162b2:三期試驗
上周,輝瑞及其德國合作夥伴BioNTech宣布,在沒有事先感染的群體中,其疫苗在預防新冠病毒方面的有效性超過90%。相比之下,按照美國CDC的數據,流感疫苗的有效率是40%至60%。
美國免疫學家福奇博士稱,輝瑞疫苗超過90%、接近95%的有效率將是說服民眾接種疫苗的關鍵因素;並稱美國可能會在12月底開始向重點人群提供疫苗。
輝瑞將在本月晚些時候向FDA提交緊急使用授權申請。
Moderna疫苗mRNA-1273:三期試驗
Moderna在上周晚些時候向投資者表示,已經完成了對其新冠疫苗首次分析的數據收集工作,預計會在本月底之前宣布該疫苗的功效,並在12月初申請緊急使用授權。
值得注意的是,Moderna和輝瑞的疫苗均采用了mRNA技術。這也是為什麽外界同樣對Moderna的疫苗有效性同樣寄予厚望。
阿斯利康疫苗AZD1222:三期試驗
9月初,因為參與三期試驗的一名英國患者出現了不明原因疾病,阿斯利康與牛津大學合作的新冠疫苗暫停了試驗。
10月23日,阿斯利康稱,在試驗擱置了一個多月後,該公司已經獲許重啟其在美國的試驗。
目前,試驗暫停對阿斯利康疫苗研發時間表的影響仍不得而知。阿斯利康此前曾表示,準備在年底之前將數據提交給FDA,申請緊急使用授權。在7月份的時候,阿斯利康公布的中期數據顯示,在所有評估的受試者中,該疫苗均被耐受,並產生針對新冠病毒的強大免疫應答。
強生疫苗Ad26.COV2.S:三期試驗
強生在9月23日成為美國第四家進入到潛在疫苗後期測試階段的製藥商。但在10月12日,該公司宣布,其涉及6萬名成年誌願者的大規模試驗因為受試者出現不明原因疾病而暫停。
約兩周後,強生宣布將恢復三期臨床試驗,因沒有證據表明其候選疫苗造成了受試病患的醫療事故。
強生此前公布的時間表是,預計將在2021年初獲得緊急使用授權。
諾瓦瓦克斯NVX-CoV2373:二期試驗
諾瓦瓦克斯在10月27日宣布,將美國的三期試驗時間推遲一個月至11月底。不過,該公司已經在英國開始了後期試驗。
按照此前的說法,諾瓦瓦克斯預計能在2021年一季度獲得申請緊急使用授權所需要的數據。
疫苗上市最利好哪些股票?
按照當前的疫苗研發速度,華爾街預計,如果進展順利,明年1月份至少會有一種疫苗在美國獲得審批,並在上半年得以在該國廣泛分發。樂觀者預計明年年中或年底,一切都會恢復至正常情況,較為悲觀的觀點則預計要到2022年才能恢復正常。
高盛在周五晚間發布的研報中指出,假設疫苗在未來幾周獲得審批,投資者可以關注一些2021年每股收益預期與2019年疫情前每股收益差距最大的股票,做多這些「深度價值股」。
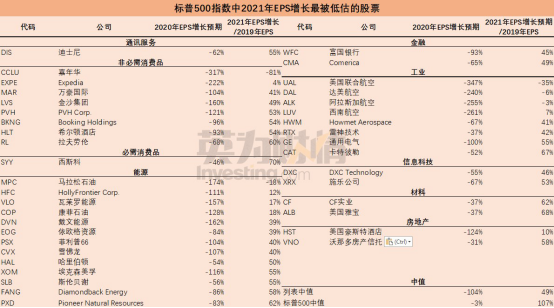
按照高盛的說法,在未來幾個月內,隨著疫苗的獲批和分發,這些企業的每股收益積極增長將超出市場的預期。三季度財報季明顯突出了企業削減成本的成效,預計在短期內企業不會重新大舉招聘,因此收入的增長料將推動利潤大幅反彈。
編輯/isaac